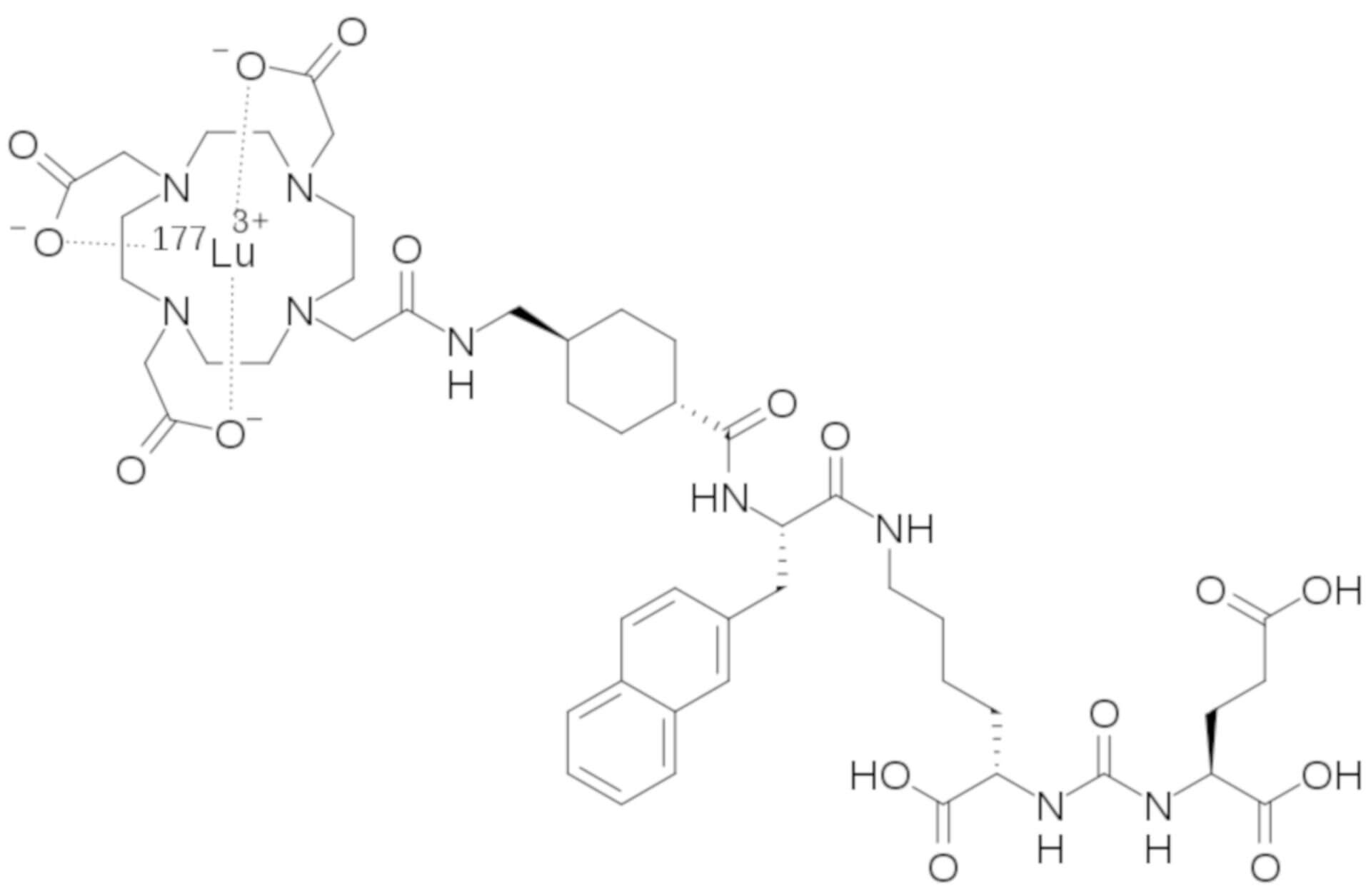
Lutetium(177Lu)vipivotidtetraxetan (177Lu-PSMA-617) ist ein Arzneistoff aus der Gruppe der Radiotherapeutika. Unter dem Namen Pluvicto (Hersteller: Novartis) ist er seit 2022 in den USA und in der EU zur Behandlung einer bestimmten Form von Prostatakrebs zugelassen.
Eigenschaften
177Lu-PSMA-617 ist ein Radioliganden-Therapeutikum. Der biologisch aktive Teil ist das Radionuklid Lutetium-177.
Die DOTA-Chelator-Verbindung PSMA-617 (Vipivotidtetraxetan, DOTA-trans-Amc-Nal-(1→6)-Lys-(N2→)-CO-Glu-OH) vermag das strahlentherapeutisch wirksame 177Lutetium-Kation durch Komplexierung zu binden. Mit dem anderen Ende bindet PSMA-617 an das prostataspezifische Membranantigen (PSMA), ein Transmembranprotein, das bei Prostatakrebs, einschließlich mCRPC, exprimiert wird. Die von Lutetium-177 abgegebene Beta-Minus-Strahlung induziert an den PSMA-exprimierenden und den umliegenden Zellen DNA-Schäden, die zum Zelltod führen.
Das Glu-CO-Lys-Strukturmotiv ist ein Baustein, der sich gut für die Entwicklung wirksamer PSMA-Inhibitoren eignet und stellt ein gemeinsames Merkmal vieler PSMA-spezifischer Radiotracer dar. Das aktive Zentrum von PSMA enthält zwei Zn2 -Ionen, zwei Untertaschen (S1 und S1′) und eine hydrophobe S1-Hilfstasche. Der PSMA-Bindungshohlraum hat einen trichterförmigen Eingangstunnel von etwa 20 Å Länge und eine Aren-Bindungsstelle an der Außenfläche des Proteins. Die hohe Affinität der Glu-CO-Lys-Einheit für PSMA beruht auf Wechselwirkungen des Glutaminsäurerests mit der S1-Bindungstasche sowie auf der Bindung der Harnstoff-Funktionalität an das aktive Zn2 -Zentrum.
Therapeutische Verwendung
Das Anwendungsgebiet von 177Lu-PSMA-617 umfasst die Behandlung erwachsener Patienten mit PSMA-positivem metastasiertem kastrationsresistentem Prostatakrebs (mCRPC), bei denen Therapieoptionen wie Taxan-basierte Chemotherapie und Behandlung mit Androgenrezeptor-Signalweg-Inhibitoren ausgeschöpft sind. Das Mittel wird als intravenöse Infusion in mehreren Zyklen verabreicht.
Klinische Prüfung
Die Zulassung beruht auf den Ergebnissen der Phase-3-Studie VISION. In dieser prospektiven, unverblindeten, aktiv kontrollierten und multizentrisch angelegten Studie wurden Patienten mit progressivem PSMA-positiven mCRPC, welche 177Lu-PSMA-617 zuzüglich zur Standardtherapie (Best Standard of Care, BSoC) erhielten, verglichen mit Patienten, die nur mit der Standardtherapie behandelt wurden.
Primäre Endpunkte für die Wirksamkeit waren das – mittels radiografischer Bildgebung ermittelte – progressionsfreie Überleben (rPFS) nach den Kriterien der Prostate Cancer Working Group 3 (PCWG3) durch eine verblindete unabhängige zentrale Überprüfung (Blinded Independent Central Review, BICR), das 8,7 Monate in der BSoC 177Lu-PSMA-617-Gruppe betrug gegenüber 3,4 Monate in der BSoC-Gruppe, sowie das Gesamtüberleben (OS) (15,3 vs. 11,3 Monate). Ein zusätzliches Maß für die Wirksamkeit war die Gesamtansprechrate (ORR) gemäß den RECISTv1.1-Kriterien.
Nebenwirkungen
Die häufigsten Nebenwirkungen, die bei mindestens 20 % der Behandelten auftraten, sind Müdigkeit, Mundtrockenheit, Übelkeit, Anämie, Appetitlosigkeit und Verstopfung. Die häufigsten Laboranomalien waren verminderte Lymphozyten, vermindertes Hämoglobin, verminderte Leukozyten, verminderte Blutplättchen sowie verminderte Calcium- und Natriumspiegel.
Entwicklung
Der Wirkstoff wurde im Deutschen Krebsforschungszentrum und im Universitätsklinikum Heidelberg entwickelt. Zur präklinischen Entwicklung wurde er an die ABX GmbH in Radeberg auslizenziert. 2017 hat die US-amerikanische Firma Endocyte Inc. die exklusiven Lizenzrechte für die Entwicklung und Vermarktung des Wirkstoffs von ABX erworben. Am 18. Oktober 2018 gab Novartis dann bekannt, Endocyte für 2,1 Milliarden US-Dollar übernehmen zu wollen.
Sonstiges
Das Arzneimittel hatte im September 2021 von der FDA einen „Priority Review“-Status erhalten und konnte somit in einem beschleunigten Verfahren im März 2022 zugelassen werden. In Deutschland kann es im Rahmen eines Härtefallprogramms (Compassionate Use) zur Anwendung kommen. Für die Länder des europäischen Wirtschaftsraumes erfolgte die Zulassung im Dezember 2022.
Literatur
- O. Sartor et al.: Lutetium-177–PSMA-617 for Metastatic Castration-Resistant Prostate Cancer. In: The New England Journal of Medicine. Band 385, 2021, S. 1091–1103, doi:10.1056/NEJMoa2107322.
- M. Lenzen-Schulte: Radioligandentherapie: Die Ultima Ratio beim Prostatakrebs. Deutsches Ärzteblatt, Bd. 114, Nr. 44, 2017; A-2036 / B-1718 / C-1683.
Einzelnachweise